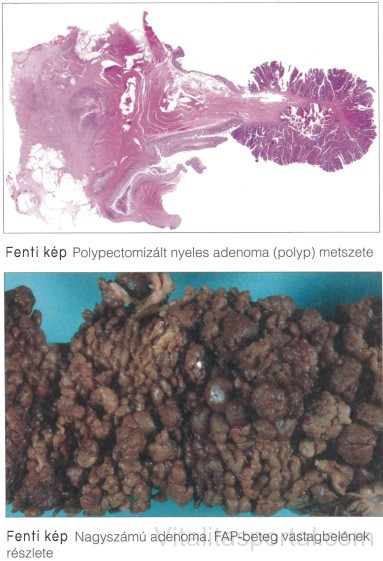
Colorectalis carcinoma – vastagbél daganat okai diagnosztikája
Definíció
A colorectalis carcinoma epithelialis eredetű, rosszindulatú daganat.
Epidemiológia
A vastagbélrák a gazdaságilag fejlettebb országokban ma a második legnagyobb halálozással járó daganat. Világszerte egy évben összesen mintegy egymillió új eset felfedezésére lehet számítani, és körülbelül félmillióan halnak meg a betegségben.
„Jóléti daganat”
A vastagbélrákot korábban „jóléti” daganatnak tartották, mivel a gazdaságilag fejlettebb országokban és a jómódúakban alakult ki elsősorban. A betegség ma is főként a fejlettebb országokra jellemző, alacsony az incidenciája Afrikában, Ázsia szegény országaiban, ugyanakkor több, korábban kevésbé érintett területen rohamosan nő az előfordulása, így például Kelet-Európában.
A szocioökonómiai helyzet tekintetében azonban az előfordulás módosult, mert az étrend, életmód (táplálkozás, mozgás) változásával az iparilag fejlettebb országokban a kockázati tényezők a szegényebb rétegeket erősebben érintik.
A CRC incidenciájában, mortalitásában jelentős (közel 25-szörös) földrajzi különbségek figyelhetők meg, amelyek ugyanakkor összefüggenek egy ország gazdasági fejlettségével. A legmagasabb incidenciaértékeket Ausztráliában, Észak-Amerikában és Japánban regisztrálták, de hasonlóak a kelet-európai, így a magyar, illetve a cseh adatok is. Száz ember közül ma Magyarországon átlagosan 6-ban alakul ki CRC.
Kulcsfontosságú megállapítások
- A vastagbélrák a gazdaságilag fejlettebb országokban a második legnagyobb halálozással járó daganat.
- A vastagbélrákok 3-4%-a öröklődő szindróma része, 20-25%-a familiáris, 70-75%-a sporadikus.
- A daganat kialakulását veleszületett vagy szerzett génmutációk akkumulációja idézi elő.
- A korai, jó prognózisú CRC-k többnyire csak szűréssel mutathatók ki.
- A CRC diagnózisában legfontosabb a kolonoszkópia és a szövettani vizsgálat.
- A helyes kezeléshez alapvető a pontos preoperatív stádiummeghatározás, ehhez korszerű képalkotó módszerek szükségesek.
- A gyógyítás legfontosabb része a sebészi kezelés, amit a stádiumtól függő pre- vagy posztoperatív kemo, radioterápia egészít ki.
- A vastagbéldaganatok átlagos ötéves túlélése a legfejlettebb országokban 65% körül van.
- A vastagbélrák-incidencia és -halálozás csökkentésének legköltséghatékonyabb módszere a szűrés.
Halálozás Magyarországon
Magyarországon a vastagbélrák halálozása 1965 és 2000 között rohamosan nőtt, azóta lényegében stagnál, illetve keveset csökken A rohamos növekedésnek minden bizonnyal elsősorban környezeti (életmód, táplálkozás) okai vannak, de szerepe van a hosszabb élettartamnak, a lakosság elöregedésének is.
A tüdőrák után a CRC a második legnagyobb mortalitású daganat. Amíg 1965-ben mintegy 1900-an haltak meg a betegségben, az utóbbi évtizedben ez a szám évi 5000 körül van. Negyven évvel ezelőtt az összes daganat 9,5%-át tették ki a vastagbéldaganatok, az utóbbi években több mint 14%-át.
Nemi érintettség
A CRC a két nemet megközelítően azonos mértékig érinti, de férfiakban több a rectumdaganat, és az előfordulás 5-10 évvel megelőzi a nőket, amit a szűrési stratégiákban is célszerű figyelembe venni. A colontumorok a jobb colonfélben viszont valamivel gyakoribbak nőkben, különösen az idősebb korosztályban.
CRC kialakulásának okai
A vastagbélrák kialakulásában genetikai és környezeti tényezők egyaránt szerepet játszanak. Az esetek 4-5%-ában ismert genetikai mutáció (FAP, HNPCC) áll a háttérben. A többi, ún. sporadikus rák esetében is 15-20%-ban kimutatható egy vagy több vérszerinti hozzátartozó érintettsége. Egy elsőfokú rokon CRC-je esetén a kockázat mintegy kétszeres, különösen, ha 50 éves kor előtt alakult ki a betegség, több rokon betegsége esetén a rizikó még nagyobb.
Környezeti tényezők
Számos környezeti tényező, illetve betegség, állapot kapcsán merült fel a CRC előfordulását elősegítő vagy gátló hatás. Az étrendi összetevőkből elsősorban a „vörös húsok”, zsír, magasabb összkalória, illetve fehérjebevitel kockázatnövelő szerepét hangsúlyozzák a nagy beteganyagot vizsgáló tanulmányok, bár ellentmondó eredmények is ismertek. Grillezett, erősen megsütött húsok esetén a kockázat nagyobb, amit a túlhevítés során keletkező rákkeltő, heterociklusos aminők, nitrozovegyületek képződése magyaráz. A zsírok közül a telített zsírsavak a veszélyesek.
Alkoholfogyasztás
A rendszeres alkoholfogyasztás növeli a CRC kockázatát. A hatás napi 40 grammnál nagyobb mennyiség tartós fogyasztása után jelentős. Az alkohol immunszuppresszív, sejtproliferációt serkentő, valamint DNS-metilációt előidéző hatása lehet a háttérben. Ismert olyan adat, amely szerint az alkoholfogyasztás fokozza a májmetasztázis esélyét. A dohányzás szerepével kapcsolatban ellentmondó adatok ismeretesek, összességében úgy tűnik, hogy kismértékben növeli a kockázatot.
Elhízás, cukorbetegség
Az obesitas, főként a centrális típusú elhízás több daganatféleség, köztük a CRC kockázatát is növeli. A fokozott veszély elsősorban férfiakban, illetve premenopauzában lévő nőkben mutatható ki. A magyarázatot a hyperinsulinaemia szerepében látják. Ugyancsak gyakoribb a vastagbélrák kialakulása diabéteszesekben, inzulinnal kezeitekben, kis mértékben kismedence-irradiáción átesettekben (nőgyógyászati tumor, prostatacarcinoma).
Kockázatcsökkentő tényezők
A protektiv étrendi tényezők közül elsősorban a gyümölcsök, zöldségfélék védő hatása tűnik meggyőzőnek. Különösen a nyers zöldségek rendszeres fogyasztása csökkenti a kockázatot. A legismertebb védő étrendi tényező a diétás rost. A feltételezett kemopreventív mechanizmus szerint a rost hígítja a béltartalmat, megköti a toxikus anyagokat, gyorsítja a tranzitidőt, csökkenti a béltartalom pH-értékét. Több, nagy megfigyeléses és polypprevenciós, prospektiv tanulmányban azonban nem tudták igazolni a rostok védő szerepét.
Betegség kifejlődése
Az utóbbi évtizedek intenzív kutatásainak eredményeképpen közelebb jutottunk a CRC kialakulásának a megértéséhez. A CRC kialakulásában genetikai és környezeti tényezők egyaránt szerepet játszanak.
Genetikai szempontból három csoport különíthető el:
- Sporadikus rákok (70-75%). A családban nem ismert vastagbéldaganat, többnyire 50 éves kor fölött indul, környezeti rizikótényezők szerepe sokszor kimutatható.
- Öröklött (herediter) rákok (3-4%). Polyposissal járó (pl. FAP), illetve polyposissal nem járó (HNPCC) formák. Obligát vagy jelentősen fokozott a vastagbéldaganat kialakulásának a kockázata.
- Familiáris vastagbélrák (20-25%). Az öröklődés genetikai szubsztrátuma nem ismert. A családban már előfordult CRC, a kockázat nagyobb, mint az átlaglakosságban, de lényegesen kisebb, mint az előző csoportban.
A colorectalis rákok nagy többsége adenomából alakul ki (adenoma – carcinomaszekvencia). A CRC kialakulása hosszú folyamat, amelynek során az ép nyálkahártyából előbb aberráns cryptafocus (ACF) keletkezik, majd a progresszió során adenoma, illetve adenocarcinoma fejlődik ki. Az ACF-ek feltételezett praeneoplasztikus léziók, amelyek patológiai szempontból a hyperplasztikus és a dysplasztikus állapot közötti átmenetet képviselik.
Mutációk kialakulása
A genetikai mutációk lehetnek öröklöttek vagy szerzettek. A fogantatás előtt kialakult mutációt csírasejtes (germline) mutációnak nevezzük, amit a szülő az öröklődés menete szerint továbbad az utódnak. Ugyanilyen mutációk spontán is kialakulhatnak a spermiumban, petesejtben, zigótában, ilyenkor a szülőben természetesen nem alakul ki a betegség. A szomatikus mutációk gyakrabban alakulnak ki később az élet folyamán. A mutáció a sejtnek szelektív növekedési előnyt biztosít a többi sejthez viszonyítva, ami a sejt clonalis proliferációját segíti elő.
A sejtekben azután második, illetve újabb mutációk alakulnak ki, halmozódnak fel, amelyek további növekedési előnyt biztosítanak. A sporadikus carcinoma kialakulása során nem egy gén hibája felelős a folyamatért, átlagosan 3-8 mutáció kell a tumor kialakulásához. A genetikai hibák felhalmozódnak a colorectalis epitheliumban, hatással vannak a növekedést reguláló génekre, fokozzák a sejtek proliferációját, és gátolják az apoptózist, ezáltal megnövelik a sejtek túlélését. A folyamat eredménye nagyszámú sejt clonalis expanziója, a szövetek dezorganizációja, invázió, metasztázisképződés. A folyamatban különböző géncsoportok mutációja vesz részt.
Az onkogének a sejtnövekedés és a sejtciklus szabályozásában szereplő fontos gének. Az onkogének mutációja a gén folyamatos, „konstitutív” aktivációjához vezet. Egy onkogén egyetlen alléljének szomatikus mutációja elégséges ahhoz, hogy a sejtnek szelektív növekedési előnyt biztosítson. A vastagbélrákok patogenezisében fontosabb onkogének: RAS, SRC, c-MYC, c-ERB B-2.
A RAS-onkogének közül a humán colorectalis karcinogenezisben legfontosabb a K-RAS, amelynek mutációja a kis adenomákban ritka, ugyanakkor a nagyobb polypok, illetve rákok mintegy felében kimutatható. Ez arra utal, hogy a RAS-mutáció viszonylag késői jelenség, a nagyobb adenomastádiumban következik be.
A tumorszuppresszor gének gátló hatásúak a sejtciklusra. Mutációjuk esetén a gének funkciója romlik, ami a normál kontrollmechanizmus kieséséhez, a sejt ellenőrizetlen növekedéséhez vezethet. Általában mindkét tumorszuppresszor gén mutációja szükséges a szelektív sejtnövekedés elindításához.
A colorectalis karcinogenezis mechanizmusa
Genetikai eltérés többféle mechanizmussal kialakulhat. A kromoszómainstabilitás egész kromoszómarészletek vesztését okozza, ami egyes gének változásához, illetve a sejtben abnormális DNS-mennyiséghez (aneuploidia) vezet. Mikroszatellita instabilitás esetén az ismétlődő DNS-szekvenciákban jönnek létre mutációk, míg a metiláció epigenetikus jelenség, amely a gén átírását (transzkripció) változtatja meg.
Az elmúlt 20 évben a molekuláris genetikai ismeretek robbanásszerű fejlődése azt igazolta, hogy a vastagbélrák kialakulásához vezető út többirányú. Nincsenek sine qua non mutációk, a karcinogenezis több, egymástól független úton létrejöhet, akár egyidejűleg, egy adott szervben is.
Patológia
A colorectalis carcinoma (CRC) diagnosztikájában, a praemalignus léziók vizsgálatában, a prognózis megítélésében, a karcinogenetikai vizsgálatokban nagy szerepe van a patológusoknak. A patológus gyakran találkozik CRC-s betegekből származó endoszkópos, biopsziás mintákkal. A praecarcinomás elváltozások kapcsán nem szabad megelégedni az elváltozások leírásával, hanem meg kell mondani az elváltozás pontos patobiológiai természetét. A dysplasia fokának megítélésére a módosított Vienna klasszifikáció alkalmas.
A tumorból végzett biopsziás minták feldolgozása során, amennyiben azok reprezentatívak, nyilatkozni kell a daganat pontos hisztológiai típusáról, a differenciáltsági fokról, a mélységi terjedésről, esetleges egyéb, a prognózist befolyásoló tényezőről (pl. nyirokér-invázióról). Rectumcarcinoma esetén a kemo-és radioterápia hatékonyságát is előre lehet jelezni bizonyos prediktív immunhisztokémai markerek vizsgálatával. A sebészi reszekátumok alapos patológiai feldolgozása szolgáltat olyan prognosztikai markereket, amelyek segítségével az 5 éves túlélés megjósolható.
Lokalizáció, előfordulása
A vastagbél daganatainak nagy része a rectumban, illetve a rectum-sigma határon helyezkedik el (61,3%), orálisan csökken az előfordulási arány: sigmabél (20,9%), colondescendens (3,2%), colontransversum (5,7%), colonascendens (4,9%), coecum (4,1%). Szinkron (egyidejű), többszörös colontumort 2-7%-ban látunk (az egyik tumor gyakran sigma/rectum kiindulású). Metakron többszörös daganat szintén 2-7%-ban fordul elő. Nem ritkán extracolicus tumorok is megfigyelhetők (nőknél emlő- és endometrium, férfiaknál gyomor- és tüdőrák mellett lymphoma).
Morfológia
Makroszkópos kép
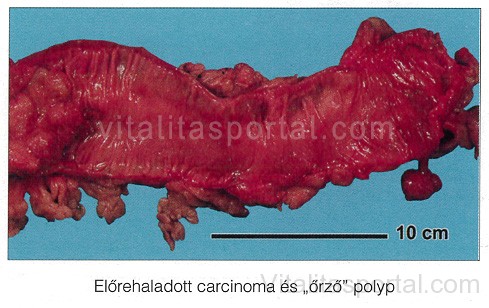
A bal colonfél előrehaladott daganatai általában körkörösek, szalvétagyűrűszerű elváltozások, szűkítik a bél lumenét, s az orális szakaszok kitágulását okozhatják. Az elváltozás szélei felhánytak, tömöttek, göbösek, felszínük közepe kifekélyesedett. Nem ritkán a daganat mellett ún. „őrző” polypot is találunk. A daganat nemcsak horizontálisan, hanem vertikálisan a bélfalban is terjed, a bélfalat perforáló erek mentén az izomrétegben és a subserosában is megtalálható. A submucosában lévő ereket beszűrve nyirokcsomókba vagy a májba adhatnak áttétet.
Az anus környéki carcinomák a vena cava ágrendsze-rén keresztül a tüdőkben okozhatnak hematogén áttétet. Ha a tumor eléri a serosát, peritonealis disszemináció lehet a következmény (carcinosis peritonei). A tumor bélfali kiterjedésén és a nyirokcsomóáttétek jelenlétén vagy hiányán alapszik a Dukes által leírt colorectalis tumor stádiumbeosztása. A módosított Astor-Coller-féle Dukes-beosztást inkább a sebészek használják.
A jobb colonfél előrehaladott daganatai poiypoid/fun-gosus jellegűek, karfiolszerűen emelkednek a bél lumenébe. Lapos, kifekélyesedő elváltozások ritkábban fordulnak elő. Ezek a tumorok általában lassabban progrediálnak, illetve később okoznak klinikai tüneteket (bélelzáródást), ti. a coecum befogadóképessége nagyobb. A jobb colonfél daganatai között több az ún. HNPCC jellegű tumor, amelynek genezise a mikroszatellita instabilitáson alapul.
Hasonlóan a rectum daganataihoz a serosa irányában növekszenek, szintén nyirokcsomó- és máj áttétet okozhatnak. Ritkán ún. diffúz-infiltráló („linitis plasticasze-rű” képet mutató) tumor képe látható az oralis bélszegmentum extrém tágulatával. Ez fiatalokban fordul elő, ha elsődleges, akkor pecsétgyűrűsejtes carcinoma van a háttérben, de nem ritkán másodlagos-metasztatikus típusról van szó (gyomor-, epehólyag- vagy emlőeredettel).
Mikroszkópos kép
A colorectalis tumorok részletes WHO hisztológiai klasszifikációja legutóbb 2000-ben készült el, ezt használjuk.
A leggyakoribb tumortípusok az alábbiak:
- Adenocarcinoma: a leggyakoribb tumortípus, amelyben tubularis, papillaris, acinaris, cribriformis részletek előfordulnak, ritkán enteroendokrin és Paneth-sejtek is kimutathatók epidermoid struktúrák mellett, még ritkábban világossejtes differenciálódás mutatkozik.
- Mucinosus adenocarcinoma: akkor mondható ki, ha a tumortömeg > 50%-a mucin, ez gyakran extracellulárisan helyezkedik el.
- Pecsétgyűrűsejtes carcinoma: a nyák intracellularisan (vakuolumban) van jelen. Fontos elkülöníteni más szervek hasonló fenotípusú daganataitól.
Klinikai kép
Bár a CRC szervezett szűrése egyre több országban elérhető, a betegség ma is leggyakrabban a tünetek alapján kerül felismerésre. Még a rendszeresen okkult vértesztszűrésen résztvevők között is az esetek felét a tünetek alapján diagnosztizálják. A szűréssel felfedezett daganatok között lényegesen magasabb a korai stádiumú tumorok aránya, mint a tünetek alapján kimutatott esetekben, ezáltal a prognózisuk is jobb.
A CRC tünetei a daganat okozta szűkülettel, érsérüléssel, a tumor toxikus hatásával, néha a peritoneális érintettséggel függenek össze, ugyanakkor nagymértékben függenek a tumor lokalizációjától, nagyságától. A vastagbéldaganatok lokalizációs megoszlása fokozatosan változik.
A korábbi nyugati adatok szerint az összes vastagbéldaganat mintegy egyharmada érintette a rectumot, egyharmada a bal colonfelet és egyharmada a jobb colont. A legújabb felmérések szerint viszont az összes tumor 55%-a már a flexura lienalistól proximálisan helyezkedik el. Magyarországon a rectumtumorok aránya még mindig megközelíti a 40%-ot.
A tüneteket célszerű csoportokba sorolni
Székeléssel kapcsolatos tünetek: székelési habitus változása: hasmenés, székrekedés, a kettő váltakozása, rectumdaganatoknál elégtelen kiürülés érzése.
- Vér ürülése a széklettel: többnyire haematochezia, de a jobb colonfél tumoraiban ritkábban melaena formájában. Az okkult vérzés inkább a jobb colonfél tumoraira jellemző, és a vérvesztés jelentősebb szokott lenni, mint distalis lokalizációban.
- Hasi fájdalom: görcsös fájdalom, tenezmus, sajnos nem ritkán a kialakuló vastagbélileus az első jelentős tünet. Bal oldali tumoroknál a szűkebb lumen és a konzisztensebb széklet miatt hamarabb jelentkezik fájdalom, míg a jobb colonfélben ez késői tünet. A jobb colonfélben a polypoid tumorok jellemzőek, míg a bal flexurától dista-lisan gyakoribbak a gyűrűszerű tumorok, a széklet konzisztensebbé válása mellett ez a fő oka az eltérő tüneti megoszlásnak.
Fájdalmat okozhat a peritoneum érintettsége, továbbá rectumtumoroknál a kismedencei izomzat, illetve idegek irritációja. Ritkább tünet a tompa, feszítő hasi fájdalom. Székeléskor a végbélben érzett fájdalom distalis tumorra, nagyon erős fájdalom a sphinctert is infiltráló tumorra utal.
Általános tünetek:
Étvágytalanság, fogyás, hányinger, hányás, vérszegénység és ennek tünetei.
Ritka tünetek:
Inkontinencia, nyákos széklet, ismeretlen eredetű láz, thromboembolia, néha az előrehaladott tumor tünetei: tapintható rezisztencia, tapintható nyirokcsomók, ascites, tumoros perforáció jelei, tumoros fisztula (hólyag, egyéb bélszakaszok felé).
Célszerű figyelembe venni, hogy a tünetek szinte soha nem önállóak, mindig legalább két-három tünet társul. A leggyakoribbak: a székelési habitus változása, rectalis vérzés, hasi fájdalom, fogyás, anaemia különböző társulása.
A tüneteknek bizonyos lokalizációs és prognosztikus jelentőségük is van. A distalis és baloldali tumorokra inkább a haematochezia, a tenezmus, a székrekedés, illetve az obstipáció és a hasmenés váltakozása, inkontinencia, jellemző, míg a proximális tumorok esetén a melaena, görcsös hasi fájdalom, fogyás, anaemia, tapintható tumor fordul elő gyakrabban.
Jelentősebb súlyvesztés, anaemia, ileus, illetve vastagbél-perforáció kedvezőtlen prognosztikus jelek, előrehaladott stádiumú daganatot jeleznek. A haematocheziával jelentkező esetek ugyanakkor jobb kimenetelűek, feltehetően azért, mert hamarabb kerül sor a diagnózisra. A rectalis vérzés prediktív értéke kifejezett életkori függőséget mutat. Amíg 50 év alatt viszonylag ritkán származik tumorból, idősebb korban az esetek egyötödében colorectalis rák van a háttérben.
Az esetek mintegy egytizede kerül sürgősséggel kórházba, többnyire ileus, ritkábban perforáció vagy masszív vérzés tünetei miatt. A felmérések szerint a betegek tünetei általában már 3-6 hónappal a diagnózist megelőzően fennálltak, és a legnagyobb késés a 40 év alatti korosztályban figyelhető meg.
A CRC diagnózisa
A CRC diagnózisának a felállítására ma még többnyire a fenti tünetek alapján, ritkábban a szűrővizsgálatok során kerül sor. A gondosan végzett anamnézisfelvétel és fizikális vizsgálat (rectalis digitális vizsgálattal!) során, a fent részletezett tünetek és eltérések alapján többnyire már előrehaladott betegséget diagnosztizálhatunk (tapintható tumor, metasztatikus máj, tumor általános tünetei). A diagnosztikában a legfontosabb a szövettani vizsgálattal kiegészített endoszkópia szerepe, a stádiummeghatározásban, az általános állapot felmérésében, követésben a képalkotó, laboratóriumi és egyéb metodikák is nélkülözhetetlenek.
Laboratóriumi vizsgálatok
A laboratóriumi vizsgálatok nem alkalmasak a betegség diagnózisára, ugyanakkor felhívhatják a figyelmet a zajló folyamatra, és tájékoztatást adnak a beteg általános állapotáról, utalhatnak a szövődményekre. A rutin laboratóriumi leletek közül az anaemia, elsősorban a mikrocitás anaemia jellemző a vastagbélrákra. Idősebb korban a vashiányos vérszegénység hátterében kb. 10%-ban derül ki CRC. A gyorsult Westergreen-érték, az emelkedett májfunkciós, különösen a cholesta-ticus enzimértékek (májmetasztázis) előrehaladottabb betegséget jeleznek.
A tumormarkerek közül a karcinoembrionális antigén (CEA) és a karbohidrát-antigén (CA) 19-9 a leghasználhatóbbak. A betegség primer diagnózisában nincs jelentőségük alacsony szenzitivitásuk és specificitásuk miatt (egyéb tumorok mellett különböző benignus kórképben is pozitívak lehetnek), a vastagbélrák szűrésére sem ajánlottak. Jelentőségük a prognózis megítélésében és a követésben van. A magas induló (preoperatív) CEA-érték előrehaladottabb stádiumot és rosszabb prognózist jelez.
A műtét után továbbra is magas érték visszamaradt tumort, normalizálódó, majd az újra emelkedő érték kiújuló betegséget jelez. Műtét előtt minden vastagbélrákos betegnél indokolt a CEA vizsgálata a prognózis, a terápiás terv és a posztoperatív követés megítéléséhez. A célzott kemoterápia eldöntéséhez az újabb protokollok a K-RAS-, EGFR-státusmeghatározást is szükségesnek tartják.
Endoszkópia
A CRC diagnosztikájában a legfontosabb módszer a kolonoszkópia, amellyel lehetőség van a daganatok, a rákelőző állapotok kimutatására a teljes vastagbélben, szövettani mintavételre, a polypusok, sőt korai rákok eltávolítására. Ezt tekintik az arany standardnak, bár szenzitivitása a colorectalis carcinomák kimutatásában 95-97%, míg az 5 mm-nél nagyobb polypok kimutatásában 90-95%.
Bár a vastagbéldaganatok nagyobbik fele szigmoidoszkóppal elérhető magasságban van, mindig törekednünk kell a teljes kolonoszkópiára. Amennyiben sztenotizáló folyamat miatt preoperatív állapotban nem lehetséges a teljes vastagbél átvizsgálása, műtét után 3-6 hónapon belül el kell végezni. Szinkron tumor (kettő vagy több, különálló, egymástól ép colonszövettel elhatárolódó daganat) a vastagbélrákok 3-5%-ában fordul elő. A szinkron polypok gyakorisága 20-30% között van.
Endoszkópos morfológia szerint a vastagbéldaganat lehet exophyticus (polypoid), exulcerált, gyűrűszerűén szűkítő, valamint diffúzán innltráló. A de novo, illetve fiat adenomából kialakuló tumorok kezdetben kisebbek, plakkszerű, felhányt szélű fekélyre emlékeztetnek. Az endoszonográfia igen hasznos módszer, főként a rectumtumorok stádiummeghatározásában. Az eszköz segíti a célzott szövetmintavételt és a minimálisan invazív terápiát is.
Képalkotó módszerek
A kolonoszkópia diagnosztikus pontossága messze meghaladja a kettős kontrasztos irrigoszkópiáét, ami akkor indokolt, ha a coecum intubációja kolonoszkóppal nem lehetséges (gyakorlott vizsgálónál ez kb. 5-8%-ban fordul elő). A CT-kolonográfia („virtuális kolonoszkópia”) diagnosztikus pontossága mind a tumorok, mind a nagyobb polypok tekintetében kezdi megközelíteni a kolonoszkópiáét, de a költségek, hozzáférhetőség és nem utolsósorban az egyidejű szövetmintavétel, illetve terápia lehetősége a kolonoszkópia mellett szólnak. A CT-kolonográfia viszont sztenotizáló elváltozás mellett is informatív, és alkalmas a teljes vastagbél megítélésére.
Differenciáldiagnózis
A vastagbélrák tünetei nem specifikusak, így számos más kórkép lehetőségétől kell elkülöníteni. A szóba jövő leggyakoribb benignus betegségek: diverticulosis, aranyér-betegség, fertőzéses bélgyulladások, idült gyulladásos bélbetegségek (colitis ulcerosa, Crohn-betegség), irritábilis bél szindróma. El kell különíteni az egyéb, hasonló tünetekkel járó malignus betegségeket, amelyek közül a vastagbélre lokalizálódók általában csak szövettanilag differenciálhatók: lymphoma, carcinoid, melanoma, metasztatikus tumorok (legtöbbször ováriumtumor).
Klasszifikáció, stádiumok
Amennyiben a vastagbélrák diagnózisát szövettannal igazoltan felállítottuk, a további teendők, a prognózis meghatározásához tisztázni kell a betegség kiterjedését, környezetéhez való viszonyát, a lokális és távoli metasztázisokat, azaz a daganat stádiumát. A definitív, végleges stádiummeghatározás (patológiai, pT: tumor, pN: nyirokcsomó, pM: metasztázis) csupán a műtéti preparátum részletes patológiai feldolgozása alapján lehetséges, így a műtét előtt klinikai stádiummeghatározást végzünk.
A jelenleg elterjedt patológiai beosztás az AJCC (American Joint Committee on Cancer) 2002-es klasszifikációja, míg a klinikai gyakorlatban általában az Astler és Coller által módosított Dukes-beosztást alkalmazzák. A klinikai stádiummeghatározás része a beteg gondos fizikális vizsgálata (hepatomegalia, lymphadenomegalia, ascites megítélése, rectalis digitális vizsgálat stb.), a laboratóriumi adatok (pl. cholestaticus májfunkciós enzimek, vesefunkció), CEA, CA 19-9 meghatározása.
A metasztáziskimutatás hagyományos képalkotó módszerei (mellkasröntgen, hasi UH), mellett az újabb, érzékenyebb és specifikusabb preoperatív eljárások (CT vagy MRI, PET/CT, endoszonográfia) végzésére is szükség lehet. A végső stádiumot az intraoperatív megítélés mellett a reszekátum vizsgálata biztosítja.
Colon, valamint proximális rectumtumoroknál a távoli metasztázisok elsődleges helye a máj, míg distalis rectumtumorok esetében a tüdő. Mivel a rectumnak nincs serosaborítása, ezért hamar infiltrálja a környező szerveket.
Kiemelkedően fontos a hasi CT- vagy MRI-vizsgálat, illetve rectumtumorok esetén a kismedencei CT, még inkább MRI-vizsgálat a tumor kiterjedésének, regionális nyirokcsomó-metasztázis, távoli metasztázis, valamint a daganattal kapcsolatos szövődmények (perforáció, fisztula, porta thrombosis stb.) tisztázására. A CT érzékenysége a fali invázió megítélésében mintegy 50%-os, a nyirokcsomó-érintettség vonatkozásában 50-70%-os. A májmetasztázisok kimutatásában a kontrasztos MRI érzékenysége jobb, mint a CT-é. A rectumtumorok esetén különösen nélkülözhetetlen a fali infiltráció és a nyirokcsomó státus pontos ismerete a kezelés megtervezéséhez.
Szűrés, prevenció, terápia és műtéti kezelés- Colorectalis carcinoma
https://vitalitasportal.com/gasztroenterologia/vastagbelrak-onkologiai-terapia/

Szerző: Griffel Tibor
Végzettség: ELTE – Eötvös Loránd Tudományegyetem. Szakterület: a szív- és érrendszeri betegségek, gasztroenterológiai betegségek és a légzőrendszeri betegségek. Jelenleg reflexológus, életmód és tanácsadó terapeuta tanulmányokat is végzek.